资讯内容 Content
心血管科医生应站在血糖管理的一线——第二届ACE常青藤论坛会议纪要
国际循环网版权所有,谢绝任何形式转载,侵犯版权者必予法律追究。
高血糖导致心血管事件的多种机制
 李小鹰 中国人民解放军总医院
李小鹰 中国人民解放军总医院
2004年瑞典Norhammar A等进行的荟萃分析显示,糖尿病是心梗和死亡最重要的独立预测因素,相对危险度高达2.4(P=0.001),相比之下,通常受到关注的高血压其相对危险度仅为1.31(P=0.21)。第64届美国糖尿病协会(ADA)年会Banting奖得主Brownlee博士曾中肯地指出——如果没有血管并发症,糖尿病将不再是一个重大的公共健康难题。
高血糖与大血管并发症的共同机制——氧化应激
目前认为,在遗传易感性的基础上,氧化应激是血管病变的启动因素,它通过激活聚ADP核糖基聚合酶(PARP)而抑制磷酸甘油醛脱氢酶(GAPDH),进而激活以下四条通路,诱发血管并发症。
多元醇途径 在三羧酸循环中,过多的葡萄糖使得山梨醇产生增加并沉积于神经纤维,发挥神经毒性作用。而且,山梨醇还可以促进果糖的生成,后者作为一种强糖化剂能够增加糖基化终末产物(AGE)及氧自由基的产生,进而促进糖尿病血管病变的发生。
己糖胺途径 葡萄糖在线粒体内先后生成6-磷酸葡萄糖、6-磷酸果糖、乙酰葡糖胺,之后进入细胞核在O-乙酰葡糖胺转移酶的作用下,与羧氨酸、丝氨酸的残基相结合,生成PA-1、TGF-β1,造成血管堵塞。
蛋白激酶C(PKC)途径 高血糖环境下二酯酰甘油生成增加,进而在PKC(β亚型和σ亚型)作用之下,生成一系列细胞因子(图3),对血管的结构和功能产生双重影响。
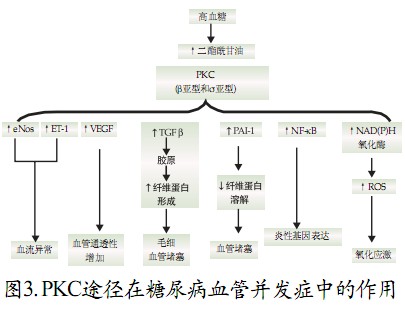
AGE途径 AGE前体通过对细胞内蛋白、细胞基质蛋白、血浆蛋白的共价修饰使其功能改变,之后与内皮细胞、系膜细胞、巨噬细胞等靶细胞膜上的AGE受体相结合,增加氧自由基、炎症介质的产生,从而加快了动脉粥样硬化的进程。
2004年欧洲糖尿病研究协会(EASD)年会Camillo Golgi大奖获得者Antonio Ceriello教授认为,过度热量摄入及运动减少使细胞内葡萄糖和游离脂肪酸浓度增高,分别引发β细胞、肌肉、脂肪组织和内皮细胞的氧化应激,进而发生动脉粥样硬化与糖代谢异常。从这个意义上说,氧化应激是引起胰岛素抵抗、糖代谢异常和心血管疾病的“共同土壤”。
阿卡波糖显著减少氧化应激
STOP-NIDDM研究结果显示,与安慰剂组相比,阿卡波糖治疗能够使IGT患者的任何心血管事件减少49%(P=0.03),使新发高血压减少34%(P=0.006)。尤其值得关注的是,阿卡波糖使心肌梗死发生率降低91%(P=0.02),提示阿卡波糖可能具有心血管保护效应,目前有证据表明这可能与阿卡波糖减少氧化应激的作用有关。
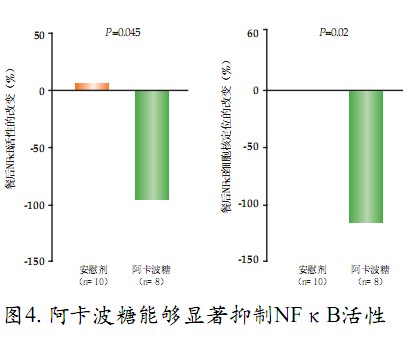
国内研究证明,阿卡波糖(150 mg/d)治疗16周使慢性炎症及氧化应激的指标——高敏CRP水平显著降低(与安慰剂组相比,P<0.01)。在另一项双盲、随机研究中,与安慰剂组相比,阿卡波糖(100 mg/d)治疗8周不仅能显著降低餐后血糖(P=0.004),还能降低餐后增强的NFκB活性(P=0.045),并抑制NFκB的细胞核定位(P=0.02)。由此可见,餐后状态可以激活炎症前机制,而阿卡波糖通过降低餐后血糖可以有效地拮抗炎症前机制所诱发的内皮功能失调(图4)。
上一页 [1] [2]